Установка Видеонаблюдения, Охранной и Пожарной сигнализации.
Звоните! Приедем быстро! Установим качественно! + гарантия 5 лет.
| Тел. ОАО «Охрана Прогресс» Установка Видеонаблюдения, Охранной и Пожарной сигнализации. Звоните! Приедем быстро! Установим качественно! + гарантия 5 лет. |
||
|
Установка технических средств охраны. Тел. . Звоните! Главная Свойства легированного феррита 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 52 53 54 55 56 57 58 59 60 61 62 63 64 65 66 67 68 0,25 МДж/м. Термически обработанные путем объемной закалки в масле рельсы обладают в 1,5-2,0 раза более высокой эксплуатационной стойкостью, чем стандартные термически необработанные рельсы, что позволяет повысить надежность железных дорог, сэкономить огромное количество металла и получить экономический эффект около-8 руб/т рельсов. Дальнейшее повышение эксплуатационной стойкости термически упрочненных рельсов может быть достигнуто легированием рельсовой стали. Перспективным является легирование углеродистой рельсовой стали небольшими добавками ванадия (~0,05 %), применение легированных сталей типа 75Х1С, 75ХГМ.Ф и др., а также применение термомеханической обработки. Часть КОРРОЗИОННОСТОЙКИЕ шестая СТАЛИ И СПЛАВЫ Глава XXI ОСНОВЫ ЛЕГИРОВАНИЯ КОРРОЗНОННОСТОЙКИХ СТАЛЕЙ Производство проката этих сталей в СССР составляет па объему около 1 %, однако себестоимость их равна 7 % от себестоимости всего проката. Поэтому выбор экономнолегированных составов коррознонностойких сталей и рациональное их применение имеют большое значение. 1. Основные понятия и определения Коррозией называется разрушение металлов и. сплавов вследствие химического или электрохимического взаимодействия их с внешней средой. В соответствии с этим различают два типа коррозии - химическую, и электрохимическую. В зависимости от свойств среды и условий взаимо действия различают следующие виды коррозии: газовую, атмо. сфериую, подводную, подземную, контактную, биокоррозию и др.; в зависимости от характера разрушения - равномерную, точечную, питтинговую, щелевую, межкристаллитную, ножевую, избира-тельную. Коррозионная стойкость - способность материала сопротивляться коррозионному воздействию среды - может определяться качественно и количественно: изменением массы образцов; объемом выде- лившегося водорода (или поглощенного кислорода); уменьшением толщины образцов; изменением показателей физических или механических свойств; плотностью тока коррозии; глубиной структурных изменений; временем до появления коррозионного очага и др. В качестве критерия коррозионной стойкости часто используют скорость коррозии, выраженную глубинным Кг (мм/год) или массовым Кы (г/м) показателями, которые связаны соотношением Кг-&,7&Кн1\ мм/год, гдеу - плотность металла (г/м). Для оценки общей коррозионной стойкости часто используют пятибалльную или десятибалльную шкалы, рекомендуемые ГОСТами. 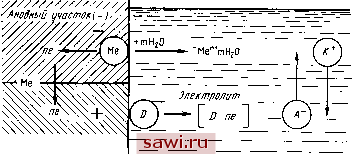 Катодный участо/<{+] Рис. 150. Схема электрохимического коррозионного процесса (Н. П. Жук) На скорость и механизм коррозионных процессов большое влияние могут оказывать внешние факторы - температуры, давление среды, напряжение, скорость потока жидкости или газа, наличие трения, кавитации, облучения. Например, под влиянием напряжений возникают явления коррозионного растрескивания (в случае постоянных растягивающих напряжений) или коррозионной усталости (под воздействием переменных нагрузок). В случае возникновения кавитации развивается коррозионная кавитация - разрушение вследствие микроударного и электрохимического воздействий агрессивной среды. Скорость коррозии конструкционных материалов под действием реакторных облучений может меняться по двум причинам: вследствие изменения свойств самого материала, когда ускорение коррозии наблюдается в связи с ухудшением защитных свойств поверхностных пленок под действием облучения, и в связи с изменением свойств теплоносителя, когда, например, в результате разложения воды и образования атомарных кислорода и водорода изменяется рН среды и скорость коррозии. В практике химическая коррозия в основном наблюдается как газовая коррозия при высоких температурах и рассматривается в разделе жаростойких сталей. Коррозионностойкие (нержавеющие) стали эксплуатируют преимущественно в условиях электрохимической коррозии (хотя в принципе не исключено и протекание химической коррозии). Коррозиоииостойкими сталями традиционно называют стали, обладающие высокой коррозионной стойкостью во влажной атмосфере и слабоагрессивных водных растворах. Стали, предназначенные для работы в средах повышенной агрессивности, называют коррозионностойкими. Согласно теории, электрохимическая коррозия развивается в ре зультате работы множества короткозамкиутых гальванических элементов, образующихся вследствие иеоднородиости металлического материа-ла или внешней среды (рис. 150). Неоднородность поверхности металлических материалов связана с различными факторами, главными из которых являются: концентрационная иеоднородиость сталей и сплавов (например, ликвация); границы зерен; присутствие в металлах различных включений; анизотропность отдельных кристаллитов; иесплошиость и различный состав поверхностных пленок; неоднородность деформаций и напряжений в металлах. Имеются также многочисленные внешние факторы (различная концентрация ионов в электролите, разные температуры, иеравиомерность внешнего электрического поля и др.), которые могут вызыиать электрохимическую гетерогенность металлической поверхности. Эффект коррозии (растворение металла) наблюдается преимущест. веиио иа анодных участках поверхности. Склонность металлов и сплавов к растворению в электролитах определяется их термодинамической устойчивостью, а также возможностью пассивации, т. е. перехода в состояние относительно высокой коррозионной стойкости, связанное с торможением анодного процесса. Возможность пассивации оценивается экспериментально получением аиодиых поляризационных кривых в условиях, когда металл, являясь анодом, может растворяться в электролите. Все коррозиониостойкие стали и сплавы пассивируются в рабочих средах, причем наиболее высокой стойкостью обладают те стали, которые имеют более широкий интервал потенциалов пассивации (и минимальное значение тока пассивации). Возникновение пассивного состояния зависит от природы металла, свойств внешней среды и действия внешних факторов (концентрации раствора, температуры, напряжений и т. д.). Имеются различные теории пассивности металлов (пленочная, адсорбционная, пассивационного барьера, электронных конфигураций и др.), что связано со сложностью явления пассивности. Наиболее полно объясняет явление пассивности н, в частности, пассивность коррозиоиностойких сталей плеиочно-адсорбционная теория, которая связывает их высокую коррозионную стойкость с образованием тонкой н плотной защитной пленки, под которой находится слой кислорода, хемо-сорбированного металлом. Кислород, концентрируясь на активных участках пленки, служит переходным слоем от металла к защитной пленке, улучшает их сцепление и переводит металл в пассивное состояние. В некоторых средах (например, в концентрированной азотной кислоте) скорость коррозии коррозионностойких сталей резко возрастает несмотря иа положительный электродный потенциал. Это явление называется перепассивацией и, по-видимому, связано с образованием в данных условиях оксидов высших валентностей, которые легко растворяются и не образуют защитных поверхностных пленок. Пластическая и упругая деформации, возникновение различных напряжений, треиие, повышение температуры и давления среды также способствуют нарушению пассивного состояния сталей. 2. Легирование коррозионностойких сталей Коррозиониостойкие (нержавеющие) стали применяют для изготовления деталей машин и оборудования и конструктивных элементов (в основном сварных),работающих в разных агрессивных средах (влажная атмосфера, морская вода, кислоты, растворы солей, щелочей, расплавы металлов и др.). Легирование коррозионностойких сталей и сплавов преследует достижение высокой коррозионной стойкости в рабочей среде и обеспечение заданного комплекса физико-механических характеристик. Легко пассивирующимися металлами являются алюминий, хром, никель, титан, вольфрам, молибден. Легирова- <Р,1 -юл -0,6
о 4 8 12 162024 О Ч 8 12 1620
20 24 28 32 36 38 ПгЩ al % СХма л\ноТ;а?о ;е За= железохромнсгых сталей с РнГ ??, * А Баба?Гов!ет. °р даще?) ние ими слабо пассивирующихся металлов, например железа, сообщает сплавам склонность к пассивации при условии образования твердых растворов. При переходе в пассивное состояние наблюдается повышение электродного потенциала, который становится более электроположительным (рис. 151,а). Такое состояние для железа наступает при содержании хрома в твердом растворе свыше 12 %, скорость коррозии снижается рис. 151,6), при этом устойчивость пассивного состояния зависит от состава коррозионной среды. Так, сталь 08X13 устойчива в растворах азотной кислоты, но корродирует в соляной и серной кислотах. Смещение электродного потенциала сплава в положительную сторону происходит и при добавках меди, платины, палладия, введение которых называется катодным легированием, что также может облегчить пассивирование сталей и сплавов. Это позволяет значительно повысить коррозионную стойкость коррозионностойких сталей во многих агрессивных средах (рис. 152). Основной легирующий элемент коррозионностойких сталей- хром. В составе применяемых в настоящее время сталей содержание хрома обычно находится в пределах от 11  12 IB 20 24 28 Cr./o Рис. 153. Влияние углерода иа положение области а; v-npeB-ращения в системе Fe-Сг-С ДО 30%. Никель в сплавах с железом повышает коррозионную стойкость в слабоокисляющих или неокисляющих растворах химических веществ, а также, как известно, стабилизирует аустенитную структуру и позволяет создать аустенитные хромоникелевые стали с высокой коррозионной стойкостью. Использование никеля в качестве основы позволяет получить сплавы с высокой коррозионной стойкостью в сильных агрессивных кислотах (соляной, серной). При создании коррознонностойких сталей для получения необходимой структуры, свойств и обеспечения максимальной коррозионной стойкости используют в различных сочетаниях также другие легирующие элементы: ферритообразу-ющие (Si, AI, Мо, W, Nb, Ti, V) и аустенитообразующие (Ni, Мп, Со, Си). Углерод, входящий во многие коррозионностойкие, особенно в инструментальные коррозионностойкие стали, существенно расширяет область существования аустенита (рис. 153). Так, 0,6 % С обеспечивает существование аустенита до содержания в стали 28% Сг. К элементам, расширяющим область -у-твердых растворов, относятся никель и марганец, однако действие марганца существенно отличается от действия никеля. Марганец может обеспечить аустенитную структуру стали только при содержании до 15 % Сг, а при более высоком содержании хрома низкоуглеродистые стали имеют двухфазную (a+v) или трехфазную (a-t-vH-°) структуру. Поэтому при необходимости иметь в сталях высокое содержание хрома для обеспечения необходимой коррозионной стойкости требуется наряду с марганцем вводить другие аустенитообразующие элементы или заменять никель марганцем лишь частично. Наиболее распространенные в технике и изученные в настоящее время коррозионностойкие стали аустенитного, аустенито-ферритного и аустенито-мартенситного классов имеют в своей основе различные комбинации систем Fe - Сг -Ni, Fe -Сг -Ni -Мп с дополнительным легированием разными элементами. При одновременном введении ферритообразующих и аустенитообразующих элементов в сталях могут наблюдаться различные структурные и фазовые соотношения. Для облегчения определения фазового состава сталей существуют структурные диаграммы, из которых наиболее распространенной является диаграмма А. Шеффлера, построенная вначале для металла сварных швов (рис. 154). По линиям, приведенным на рисунке, подсчитываются эквиваленты, которые учитывают аустенитообразующее и 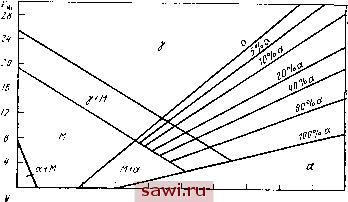 Ч 8 12 16 20 24 2в Рис. 154. Структурная диаграмма для нержавеющих, литых хромоиикелевых сталей (А. Шеффлер) ферритообразующее действие различных элементов. Аустенитообразующее действие сравнивается с никелем, а ферритообразующее - с хромом. Подсчет эквивалентов (£i(, и £ Сг) позволяет получить точку на диаграмме, попадающую в ту или иную фазовую область. Например, требуется оценить фазовый состав стали 20Х13Н4Г9. Для нее: £сг=%Сг=13; (43) £,= % Ni + 30% С + 0,5% Мп = -4+ 30-0,2 +0,5-9= 14,5. (44) Обращение к рис. 154 позволяет определить, что сталь относится к аустенито-мартенситному классу. Одна из поздних структурных диаграмм коррозионно-стойких сталей, предложенная Я. М. Потаком и Е. А. Сага-левич и применимая к закаленным сталям, приведена на Установим охранное оборудование. Тел. . Звоните! |