Установка Видеонаблюдения, Охранной и Пожарной сигнализации.
Звоните! Приедем быстро! Установим качественно! + гарантия 5 лет.
| Тел. ОАО «Охрана Прогресс» Установка Видеонаблюдения, Охранной и Пожарной сигнализации. Звоните! Приедем быстро! Установим качественно! + гарантия 5 лет. |
||
|
Установка технических средств охраны. Тел. . Звоните! Главная Свойства легированного феррита 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 52 53 54 55 56 57 58 59 60 61 62 63 64 65 66 67 68 (14) постоянная; Г-абсолютная температу- зионный поток протекает из областей с меньшей концентрацией данного элемента в области с более высокой его концентрацией. В общем виде движущей силой диффузионных процессов является не градиент концентрации, а градиент химического потенциала или свободной энергии {dGi/dx) Ji-D{dGildx). (12) Истинный коэффициент диффузии 0 = Овфф (datldx) ]-\ (13) где V - молярный объем фазы. При легировании феррита и аустенита изменяется свободная энергия углерода, которая связана с его активностью: G = /?r In ас, где - газовая ра, К. Чтобы оценить влияние легирующего элемента на активность углерода в легированном твердом растворе а за состояние сравнения выбирают активность углерода в нелегированном железе ас .имеющем тоже содержание углерода. Тогда изменение свободной энергии составит AG = RT In [allас) == RT In (vS iVc/vc Nc) = RT\n{yilyc)--RT\nfc. (15) Отношение коэффициентов термодинамической активности углерода в легированном и нелегированном железе (7 с /V с ) представляет собой относительный коэффициент термодинамической активности углерода fc- Он характеризует влияние легирующего элемента на активность угле--рода в железоуглеродистом сплаве. Если f с>1, а Infc имеет знак + , легирующий элемент повышает активность углерода в феррите и аустените, если же fc <1 ( Infc имеет знак - ), то легирующий элемент, наоборот, понижает активность углерода в твердом растворе. Изложенное дает основание считать, что диффузионный поток углерода в сплаве, определяемый градиентом свободной энергии, зависит от изменения относительного коэффициента термодинамической активности: J=~DRT{dlnfldx). (16) К настоящему времени накоплен большой экспериментальный материал по влиянию легирования на термодинамическую активность углерода в аустените и относительно мало данных об активности углерода в легированном феррите. Это связано со значительными экспериментальными трудностями определения относительного коэффициента термодинамической активности углерода в феррите из-за значительно меньшего предела растворимости углерода в нем по сравнению с аустенитом. Физическая сущность изменения коэффициента fc как в феррите, так и в аустените одна и та же и состоит в том, что легирующие элемен- ты, находящиеся в раст- f/r у,.з воре, изменяют силы свя- - зи или прочность связи между атомами металла и углерода. Карбидооб-разующие элементы будут увеличивать прочность связи углерода с атомами легирующего элемента в твердом растворе, они повышают вероятность нахождения атомов углерода в междоузлиях вблизи узлов решетки, занятых атомами легирующего карби- дообразующего элемента, притягивают к себе атомы углерода и понижают подвижность углерода в твердом растворе, то есть уменьшают его термодинамическую активность. Некарбидо- образующие элементы, замещающие атомы железа твердом растворе, будут, наоборот, отталкивать атомы углерода, повышать их подвижность, т. е. увеличивают его термодинамическую активность, при этом будет проявляться тенденция к выделению углерода из твердого раствора. Обобщенные по данным различных исследователей данные о влиянии легирующих элементов на относительный коэффициент термодинамической активности углерода в аустените приведены на рис. 28. Чем сильнее карбидообра- 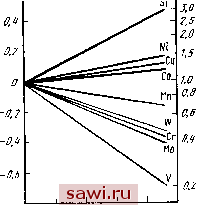 а02 0,04 0,06 0,08 0.10 Njj,:, Рис. 28. Влияние концентрации мольной доли (Wji ) различных легирующих элементов на относительный коэффициент термодинамической активности углерода в аустените tfj- ) прн 1000 °С (Ареннус) зующая способность легирующего элемента, т. е. чем левее по отношению к железу находится d-переходный металл в периодической системе, тем в большей степени понижается /с<1. Некарбидообразующие элементы в аустените Со, Ni, Si увеличивают значения /с >1. Подобные данные для феррита имеются лишь по влиянию кремния. Влияние легирующих элементов на термодинамическую активность углерода в аустените имеет большое значение в таких процессах, как растворение карбидов, нитридов и карбонитридов в аустените, выделение их из твердого раствора при охлаждении, перераспределение элементов между фазами в процессе термической обработки. В заключение необходимо отметить, что легирующие элементы оказывают влияние на термодинамическую активность углерода в твердом растворе лишь в том случае, если они растворены в этом твердом растворе, т. е. при определении возможности протекания того или иного процесса благодаря изменению термодинамической активности необходимо учитывать содержание легирующих элементов, растворенных в твердом растворе, а не их общее содержание в стали. Глава V КАРБИДЫ И НИТРИДЫ Основными фазами-упрочнителями в сталях являются карбиды, нитриды и комплексные соединения на их основе - карбонитриды. Физическая природа и свойства этих фаз во многом определяют их поведение в стали. 1. Общие закономерности Карбиды и нитриды относятся к фазам внедрения и образуются между d-переходными металлами и соответственно углеродом и азотом. На рис. 29 в последовательности, отвечающей положению металлов в периодической системе элементов, приведены обобщенные данные о кристаллической структуре и электронном строении d- и s-оболочек переходных металлов, используемых для легирования сталей, а также сведения о кристаллической структуре и стехиометриЧеской фор-
£0 &ава II It iliii -III a □ □ □ < H □ □ a □ □  □ □ □ □ □ муле карбидов и нитридов, образуемых этими элементами в сталях. Прочность связи в карбидах и нитридах между атомами металла и неметалла (межатомные силы взаимодействия) определяется строением s- и d-электронных оболочек. Для d-переходных металлов характерна (по Полин-гу) гибридизация электронов между d- и s-орбиталями, т. е. взаимопереходы электронов с одного уровня на другой. Незавершенность строения этих электронных оболочек способствует тому, что эти металлы восприимчивы к приобретению электронов из других источников. Такими источниками -донорами электронов для переходных металлов становятся атомы внедрения углерода и азота, имеющие соответственно четыре или три электрона. Эти электроны усиливают гибридизацию и увеличивают связь металл Me - неметалл Х:Ме - Х. В каждом периоде при увеличении атомного номера d-переходного металла (слева направо, например, от Ti к Ni) увеличивается заполненность электронных оболочек металла и, следовательно, силы связи или прочность связи Ме - Х будет уменьшаться. Прочность связи между атомами металла и неметалла в карбидах и нитридах характеризуют теплотой образования АЯ298К . кДж/(г-атом) и свободной энергией образования (ДОгэвк . кДж/(г-атом) фаз, температурой их плавления и структурно-нечувствительными упругими свойствами (табл. 1). Наиболее высокие значения из указанных свойств имеют карбиды и нитриды элементов IV и V групп. По мере увеличения номера группы свойства изменяются в сторону уменьшения прочности связи атомов в карбиде и нитриде или, как говорят, прочности или стойкости карбидов и нитридов. Следовательно, переходные металлы по их сродству к углероду и азоту, прочности и стойкости карбидов и нитридов, их устойчивости к распаду можно расположить в следующий убывающий ряд: Hf, Zr, Ti, Та, Nb, V, W, Mo, Cr, Mn, Fe. При образовании фаз внедрения ионизации атомов в карбидах и нитридах не наблюдается, между атомами со- На рнс. 29 приведены лишь наиболее часто встречаемые в стали карбиды и ннтрнды. В редких случаях возможно образование фаз н другого типа (например, гексагонального ннтрнда NbjN в малоперлнтных азотистых сталях нлн гексагонального карбида УгС в высоколегированных нержавеющих схалях с ннзкнм содержанием углерода). Таблица 1. Некоторые свойства карбидов и нитридов Фаза
НУ,МПа.10 Карбиды Сг,Сз СггзСб MozC МпзС МпгзСб РезС M02N Fe.N
IV V VI VIII 2950 2980 2050 2050 3090 1450 895 Нитриды -336,8 -365,4 -369,4 -175,8 -237,8 -251,2 -118,0 -69.5 -35,6 -4.6 -308,2 -337,0 -340,0 -157,8 -209,3 -222,7 -85,8 -50,2 -23,0 4-7,3 29 27 18 16 10 14,79 20,85 14,5 19 15,1 15,2 13,69 10,6 10,83 храняется металлический характер связи и эти фазы обладают металлическими свойствами. Анализ данных рис. 29 показывает, что кристаллические решетки карбидов и нитридов во всех случаях отличаются от кристаллических решеток соответствующих переходных металлов, при этом можно отметить ряд закономерностей. Для чистых переходных металлов при движении вдоль периода слева направо (от Ti к Ni), т. е. по мере заполнения внешних d- и s-электронных оболочек, происходит переход от о. ц. к. решетки к г. ц. к. и г. п. у. решетке. Карбиды и нитриды металлов IV и V групп имеют простые г. ц. к. решетки типа NaCl, у карбидов и нитридов VI периода преобладают гексагональные решетки. Карбид хро- Установим охранное оборудование. Тел. . Звоните! |